2024年上半年获批1类新药一览
据不完全统计,2024年上半年,我国共批准1类新药26个,涉及阿尔茨海默病、2型糖尿病、非小细胞肺癌、骨髓瘤、黑色素瘤等多个适应症。药品名称企业名称批准日期适应症仑卡奈单抗注射液卫材药业1月9日阿尔茨海默病儿茶上清丸齐进药业1月9日口腔溃疡脯氨酸加格列净片惠升生物1月19日2型糖尿病富马酸泰吉利定注射液恒瑞医药1月31日术后疼痛可伐利单抗注射液罗氏2月7日血红蛋白尿剂九味止咳口服液卓和药业2月21
据不完全统计,2024年上半年,我国共批准1类新药26个,涉及阿尔茨海默病、2型糖尿病、非小细胞肺癌、骨髓瘤、黑色素瘤等多个适应症。药品名称企业名称批准日期适应症仑卡奈单抗注射液卫材药业1月9日阿尔茨海默病儿茶上清丸齐进药业1月9日口腔溃疡脯氨酸加格列净片惠升生物1月19日2型糖尿病富马酸泰吉利定注射液恒瑞医药1月31日术后疼痛可伐利单抗注射液罗氏2月7日血红蛋白尿剂九味止咳口服液卓和药业2月21
多奈单抗Donanemab(商品名:Kisunla)是由跨国药企礼来(Lilly)研发的一款针对阿尔茨海默病(AD)的新药,2024年7月2日在美国正式上市。一、基本信息研发公司:礼来(Lilly)商品名:Kisunla药物类型:抗淀粉样蛋白β(Aβ)单克隆抗体批准机构:美国食品药品监督管理局(FDA)批准时间:2024年7月2日用途:用于治疗早期症状性阿尔茨海默病,包括轻度认知障碍(MCI)患者
西妥昔单抗(Cetuximab)是一种针对表皮生长因子受体(EGFR)的IgG1单克隆抗体,是用于结直肠癌等恶性肿瘤的靶向治疗药物,德国默克里昂制药公司研发。2024年6月18日,由泰州迈博太科药业有限公司研发的西妥昔单抗β注射液,经国家药品监督管理局批准在国内上市,成为首个上市的国产西妥昔单抗产品。其商品名为“恩立妥”(研发代号:CMAB009),适应症为与FOLFIRI(亚叶酸、5FU和伊立替
1类创新药考格列汀片(商品名:倍长平)是海思科自主研发、具有全球首创性的超长效口服降糖药,2024年6月25日,海思科发布公告称,已收到国家药品监局下发的《药品注册证书》,考格列汀片正式上市。公告信息显示,考格列汀片疗效和安全性与日制剂相当,10mg半衰期为131.5h、DPP-4抑制持久(给药14天后对DPP-4平均抑制率达80%以上)、药物相互作用少、在轻中度肝、肾功能损伤患者中也无需调节剂量
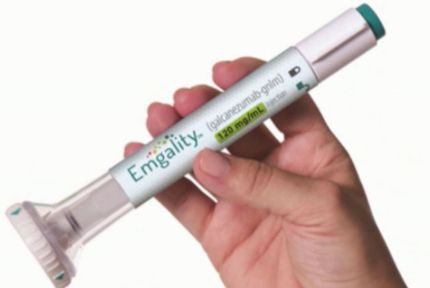
美国制药巨头礼来(Eli Lilly)偏头痛新药Emgality(galcanezumab)近日在欧盟监管方面迎来重大喜讯。欧盟委员会(EC)已批准Emgality注射液用于成人偏头痛的预防性治疗,具体为每月经历至少4天偏头痛的成人患者。Emgality将为欧洲的偏头痛成人患者群体提供每月一次、自我注射的皮下注射药物。在美国,Emgality已于今年9月底获得FDA批准。此次批准,使Emgalit
本周五,美国食品药品管理局(FDA)批准Gazyva(Obinutuzumab)与苯丁酸氮芥联合用药用于治疗之前未经处理的慢性淋巴细胞性白血病(CLL)。CLL是一种血液及骨髓疾病,该疾病通常会慢慢恶化。根据美国国家癌症研究所提供的信息,今年将有15680美国人被确诊患有这种疾病,而4580人将会死于这种疾病。Gazyva通过帮助免疫系统中某些细胞攻击癌症细胞而起作用。Gazyva是首款以突破性治
印度最高法院法官9月30日宣布暂停国家临床试验。根据裁决,在印度进行的所有药物临床试验必须被叫停两个星期。印度最高法院已经给政府一个月的时间,制定出一项新药临床试验法规,以加强监管。争议已久近年来,印度已经成为来自英国、美国和欧洲跨国制药公司进行临床试验的首选目的地,低成本和大量的研究参与者是跨国制药公司在印度进行新药临床试验的主要动力。然而,跨国制药公司在获得丰厚回报之时,参加试验的印度人民可能
早期临床研究中的风险控制是创新药临床研发中十分重要和关键的要素。为更好地引导行业科学、规范地开展创新药物的早期临床研究,有效控制风险,药审中心在国家“重大新药创制”科技重大专项“大品种药物Ⅳ临床试验及新药临床试验审评研究技术平台”课题中,将制定“早期临床研究的风险控制技术指南”列入子课题。为此,药审中心于2013年10月14日组织部分课题组相关人员赴上海复旦肿瘤医院和上海精神卫生中心进行实地调研。